羧酸是一类来源广泛、价格低廉和可再生的化学原料,满足可持续化学转化的需求。以羧酸活化酯为底物的脱羧偶联反应已被用于高附加值化合物的制备(图1A)。然而,由于羧酸非常稳定,这类方法通常依赖于金属或光催化剂降低反应能垒,并通过单电子转移(SET)实现脱羧偶联。近年来,NADH类似物的EDA结合物被发现在可见光激发下可以产生自由基,并与受体结合得到偶联产物(图1B)。这一路径虽然避免了使用金属,但这种EDA复合物介导的方法仍然需要光照来促进单电子转移(SET)过程,这在工业应用中会带来设备和能源成本方面的挑战。
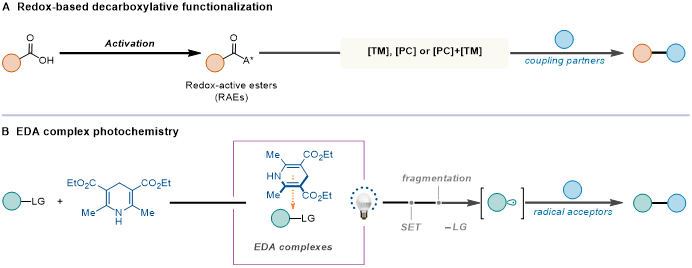
图1 羧酸到高附加值分子的合成方法
针对上述挑战,我校新药合成团队联合清华大学深圳国际研究生院毛润泽团队合作发展了一种NADH类似物促进的自由基生成新策略,在空气氛围中/非光照条件下实现了氧化还原活性酯(RAEs)的脱羧转化,为羧酸向高附加值产物的绿色高效转化提供了一种高效和简便的途径(图2)。

图2 非光照条件下NADH类似物促进的脱羧转化
该反应体系操作极为简便,将羧酸高碘酯(ADs),NADH模拟物和偶联试剂混合搅拌反应5分钟,即可得到目标分子。反应还显示出了广泛的底物普适性,可用于氨基酸、药物分子及天然产物等生物活性分子的后期修饰,为生物活性分子化合物库的快速构建提供了一种高效的手段。生物活性分子的克级实验也显示出了良好的结果,凸显了反应体系的工业化应用前景。
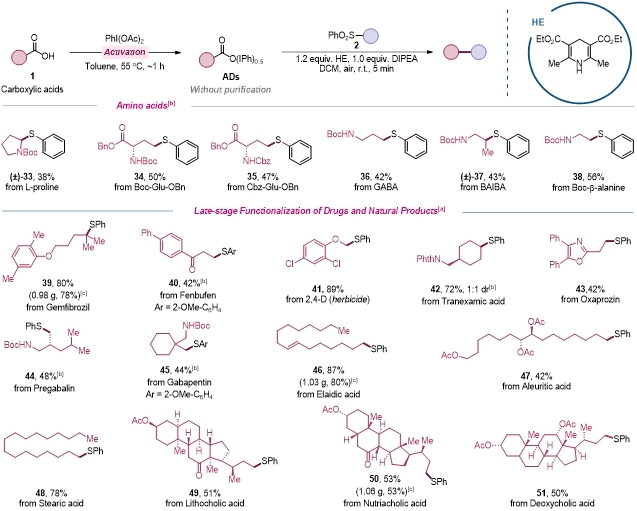
图3 生物活性分子的后期修饰
值得注意的是,通过使用其它类型的偶联试剂,原有反应体系还可以应用于其它多种化学键的构筑,包括C–X键(X = S、Se、SCF3和CN)、C–C(sp)键、C–C(sp²)键以及C–C(sp³)键(图4)。
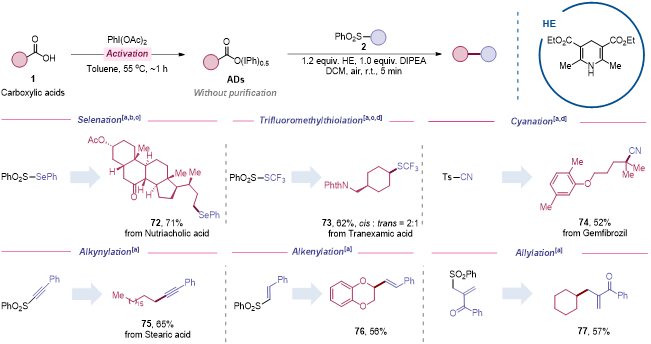
图4 多类型官能团转化
研究团队通过自由基捕获、自由基钟、环丙烷开环、关键中间体分离、密度泛函理论(DFT)计算和循环伏安法测试等手段对反应机理进行了研究,并提出了可能的反应机制。脱羧官能化途径始于PhI(OAc)2对烷基羧酸I进行原位活化,生成相应的苯碘(III)二羧酸酯II。随后,II与汉斯酯(HE)发生单电子转移(SET)过程,生成两种自由基物种:II•–、HE•以及质子H+。自由基II•–会迅速脱去CO2,生成烷基自由基III。接下来的步骤涉及SOMO-philes试剂IV捕获烷基自由基III,生成苯磺酰自由基V和目标产物VI。最后,苯磺酰自由基V与HE•发生氢原子转移(HAT)反应,最终生成吡啶83和苯磺酸84。详细内容请参考原文。
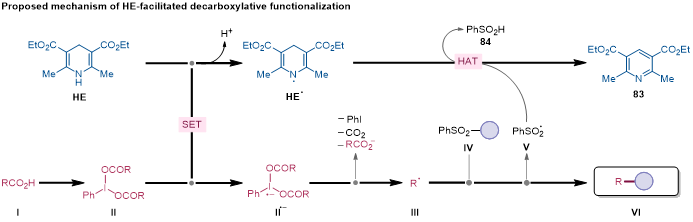
图5 反应机理
相关研究以“NADH Analogues Enable Metal- and Light-Free Decarboxylative Functionalization”为题在化学类顶级国际期刊《Angewandte Chemie International Edition》(《德国应用化学》)上发表。这是我校首次以第一单位在《Angewandte Chemie International Edition》上发表研究论文,我校化学化工学院梁磊副教授为该工作第一作者,牛红英教授为共同通讯作者。近年来,学校大力实施“质量立校、人才强校、科技兴校”战略,高质量学术成果不断涌现,标志着学校在学科建设、科技创新、青年科技人才培养和学术影响力取得了长足进展。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202415131
(图片:梁磊 初审:韩亚飞 复审:杨理 余昊 终审:许光日 刘润强)